Nilalaman
Tinutukoy ng porsyento na masa ang porsyento ng bawat elemento na bumubuo ng isang compound ng kemikal. Upang mahanap ang halagang ito, kakailanganin mo ang masa ng molar ng mga sangkap ng tambalan sa gramo / mol o ang bilang ng gramo na ginamit upang likhain ang solusyon. Ang porsyento ng masa ay maaaring kalkulahin sa isang simpleng paraan gamit ang isang pangunahing pormula na hinahati ang masa ng elemento (o solute) ng masa ng tambalan (o solusyon).
Mga hakbang
Paraan 1 ng 2: Paghanap ng porsyento ng masa sa mga naibigay na masa
- Tukuyin ang equation para sa porsyento na masa ng isang compound. Ang pangunahing pormula para sa isang compound ay: porsyento ng mass = () x 100. Dapat mong i-multiply ang resulta ng 100 sa dulo upang maipahayag ang mga halaga bilang mga porsyento.
- Ang masa ng isang compound ng kemikal kung saan ka interesado ay ang masa na ibinigay sa problema. Kung ang halagang ito ay hindi ibinigay, sumangguni sa sumusunod na Paraan at alamin kung paano makahanap ng porsyento ng masa kung hindi ibinigay ang masa.
- Ang kabuuang masa ng isang compound ay kinakalkula sa pamamagitan ng pagdaragdag ng masa ng lahat ng mga sangkap na ginamit upang likhain ang tambalan o ang solusyon.
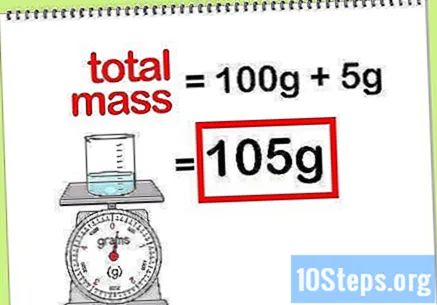
Kalkulahin ang kabuuang masa ng tambalan. Kapag alam mo ang halaga ng masa ng lahat ng mga elemento o compound na idinagdag, kailangan mo lamang idagdag ang mga ito upang makalkula ang dami ng tambalan o ang pangwakas na solusyon. Ang halagang ito ang magiging denominator sa pagkalkula ng porsyento ng masa.- Halimbawa: Ano ang porsyento ng mass ng 5 g ng sodium hydroxide na natunaw sa 100 g ng tubig?
- Ang kabuuang masa ng compound ay ang dami ng sodium peroxide kasama ang dami ng tubig: 100 g + 5 g, na kabuuan ng isang bigat na 105 g.

Tukuyin ang dami ng pinag-uusapang kemikal. Kapag kailangan mong hanapin ang porsyento ng masa, nais ng problema na hanapin mo ang masa ng isang tukoy na elemento (ang sangkap na pinag-uusapan) bilang isang porsyento ng kabuuang masa ng lahat ng mga elemento. Tandaan ang dami ng pinag-uusapang elemento. Ang halagang ito ay ang magiging bilang sa pagkalkula ng porsyento ng masa.- Halimbawa, ang dami ng elemento ay 5 g ng sodium hydroxide.
- Palitan ang mga variable sa porsyento ng pormula ng masa. Matapos matukoy ang mga halaga para sa bawat variable, palitan ang mga ito sa equation.
- Halimbawa: porsyento ng mass = () x 100 = () x 100.

Kalkulahin ang porsyento ng masa. Ngayon na nabuo ang equation, lutasin lamang ito upang makalkula ang porsyento ng masa. Hatiin ang masa ng elemento sa kabuuang masa ng tambalan at paramihin sa 100. Ang resulta ay ang porsyento ng masa ng sangkap na kemikal.- Halimbawa: () x 100 = 0.04761 x 100 = 4.751%. Samakatuwid, ang porsyento na masa ng 5 g ng sodium hydroxide na natunaw sa 100 g ng tubig ay 4.751%.
Paraan 2 ng 2: Paghanap ng porsyento ng masa sa mga masa na hindi ibinigay
- Tukuyin ang equation para sa porsyento na masa ng isang compound. Ang pangunahing pormula para sa porsyento na masa ng isang compound ay: porsyento ng dami = () x 100. Dapat mong i-multiply ang resulta ng 100 sa dulo upang maipahayag ang mga halaga bilang mga porsyento.
- Kapag hindi mo alam ang mga halagang masa, mahahanap mo ang porsyento ng mass ng isang elemento ng compound gamit ang molar mass.
- Halimbawa: Ano ang porsyento ng dami ng hydrogen sa isang Molekyul na tubig?.
Isulat ang pormula ng kemikal. Kung ang mga formula ng kemikal para sa bawat compound ay hindi naibigay, kakailanganin mong isulat ang mga ito. Kung hindi man, laktawan ang Hakbang na "Hanapin ang masa ng bawat elemento".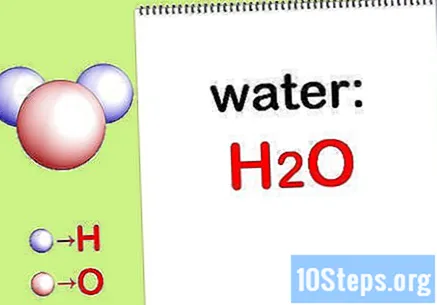
- Halimbawa, isulat ang pormulang kemikal para sa tubig: H2ANG.
Hanapin ang masa ng bawat elemento sa compound. Hanapin ang bigat ng molekular ng bawat elemento ng mga formula ng kemikal sa pamamagitan ng pagtukoy sa pana-panahong talahanayan. Pangkalahatan, ang masa ng isang elemento ay matatagpuan sa ibaba ng simbolo ng elemento ng kemikal. Tandaan ang mga masa ng bawat elemento ng tambalan.
- Halimbawa, ang molekular na masa ng oxygen ay 15.9994, at ang hydrogen ay 1.0079.
I-multiply ang masa sa ratio ng molar. Tukuyin kung gaano karaming mga moles ng bawat elemento ang nasa kemikal na tambalan. Ang bilang ng mga moles ay ibinibigay ng naka-subscribe na bilang ng compound. I-multiply ang molekular na masa ng bawat elemento ng molar ratio.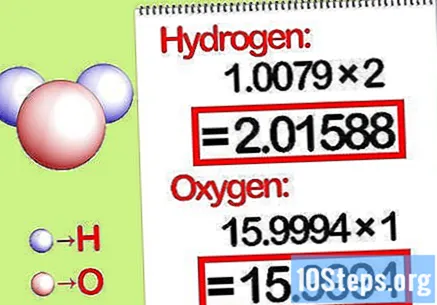
- Halimbawa, ang molar ratio ng hydrogen sa oxygen sa tubig ay 2: 1. Samakatuwid, paramihin ang bigat na molekular ng hydrogen ng dalawa (1.00794 X 2 = 2.01588) at iwanan ang molekular na bigat ng oxygen na ito ay (15.9994).
Kalkulahin ang kabuuang masa ng tambalan. Idagdag ang kabuuang masa ng lahat ng mga elemento ng compound. Gamit ang masa na kinakalkula ng molar ratio, posible na kalkulahin ang kabuuang masa ng tambalan. Ang numerong ito ang magiging denominator ng porsyento ng equation ng masa.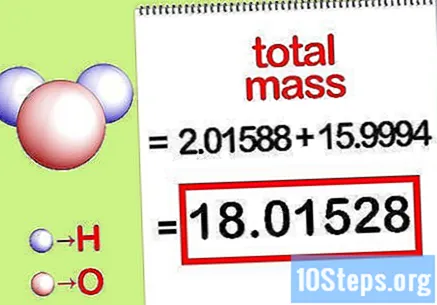
- Halimbawa, magdagdag ng 2.01588 g / mol (ang dami ng dalawang mol ng mga hydrogen atoms) na may 15.9994 g / mol (ang bigat ng isang solong nunal ng isang oxygen atom) at kumuha ng 18.01528 g / mol.
Tukuyin ang dami ng pinag-uusapang elemento. Kapag kailangan mong hanapin ang porsyento ng masa, nais ng problema na hanapin mo ang masa ng isang tukoy na elemento sa isang compound bilang isang porsyento ng kabuuang masa ng lahat ng mga elemento. Kilalanin ang dami ng pinag-uusapang elemento at isulat ito. Ito ang halaga ng masa na kinakalkula gamit ang molar ratio. Ang halagang ito ay ang numerator ng porsyento ng equation ng masa.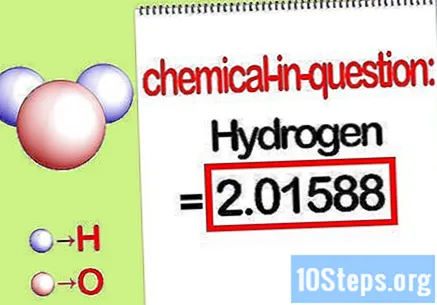
- Halimbawa, ang hydrogen mass ng compound ay 2.01588 g / mol (ang dami ng dalawang mol ng mga hydrogen atoms).
- Palitan ang mga variable sa porsyento ng pormula ng masa. Matapos matukoy ang mga halaga para sa bawat variable, palitan ang mga ito sa equation na tinukoy sa unang hakbang: porsyento ng masa = () x 100.
- Halimbawa: porsyento ng mass = () x 100 = () x 100.
Kalkulahin ang porsyento ng masa. Ngayon na nabuo ang equation, lutasin lamang ito upang makalkula ang porsyento ng masa. Hatiin ang masa ng elemento sa kabuuang masa ng tambalan at paramihin sa 100. Ang resulta ay ang porsyento ng masa ng sangkap na kemikal.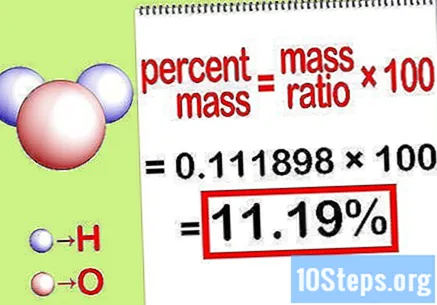
- Halimbawa, porsyento ng mass = () x 100 = 0.111189 x 100 = 11.18%. Kaya, ang porsyento ng dami ng mga atomo ng hydrogen sa isang Molekyul na tubig ay 11.18%.